細胞死亡的神秘世界迎來新成員,鐵死亡以其獨特的鐵依賴性和脂質過氧化特征,在癌癥治療與疾病干預領域開辟了新戰場。
鐵死亡(Ferroptosis)是一種鐵依賴性、脂質過氧化驅動的程序性細胞死亡形式,自2012年正式命名以來,已成為腫瘤抑制、神經退行性疾病及代謝性疾病研究的熱點。與凋亡、壞死不同,鐵死亡在細胞形態學、生物化學和遺傳學上具有獨特特征,主要表現為線粒體收縮、膜密度增加和脂質過氧化物積累。本文將系統解析鐵死亡的核心信號通路、關鍵調控因子、先進研究策略及靶向治療前景,為相關研究提供全面指導。
一、鐵死亡的核心生化基礎
鐵死亡的發生依賴于三個關鍵生化過程:鐵代謝失衡、脂質過氧化和抗氧化防御系統失效。這三個過程相互交織,共同構成了鐵死亡的核心生化基礎。
鐵作為芬頓反應(Fenton reaction)的催化劑,能將過氧化氫轉化為高活性的羥基自由基,進而引發脂質過氧化。正常情況下,細胞內鐵穩態通過轉鐵蛋白受體(TfR)、鐵泵蛋白(FPN)等精密調控。當細胞內二價鐵(Fe2?)過量積累時,會通過芬頓反應產生大量活性氧(ROS),攻擊細胞膜上的多不飽和脂肪酸(PUFAs)。PUFAs在酰基輔酶A合成酶長鏈家族成員4(ACSL4)和溶血磷脂酰膽堿酰基轉移酶(LPCAT3)的作用下合成多不飽和脂肪酸磷脂(PUFA-PLs),隨后被脂氧合酶氧化生成磷脂過氧化物(PUFA-PL-OOHs),最終導致細胞膜破裂和細胞死亡。
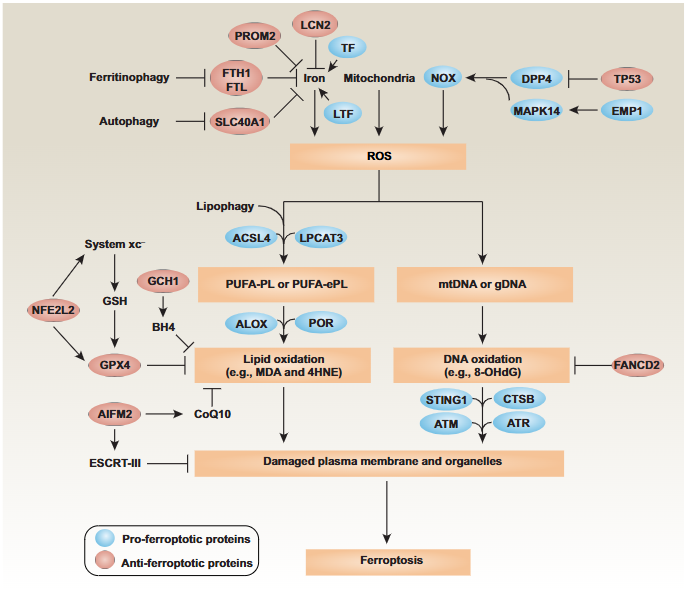
圖1 鐵死亡信號通路[1]
二、關鍵信號通路網絡
1、GPX4核心調控通路
谷胱甘肽過氧化物酶4(GPX4)是鐵死亡最核心的負調控因子。GPX4依賴谷胱甘肽(GSH)將脂質過氧化物還原為無害的脂質醇,從而抑制脂質過氧化積累。胱氨酸/谷氨酸逆向轉運體系統Xc-(由SLC7A11和SLC3A2亞基組成)負責將胞外胱氨酸轉運入胞,同時將谷氨酸轉運出胞。胞內胱氨酸隨后還原為半胱氨酸,用于GSH合成。當系統Xc-活性被抑制(如使用Erastin),或GPX4活性被直接抑制(如使用RSL3),都會導致GPX4功能喪失,引發鐵死亡。
2、非GPX4依賴的備份系統
近年來研究發現,鐵死亡還存在GPX4非依賴的調控機制:
鐵死亡抑制蛋白1(FSP1) 通過催化泛醌(CoQ)轉化為泛醇(CoQH2),后者直接中和脂質自由基,在質膜上形成獨立的抗氧化系統。
GTP環化水解酶1(GCH1) 產生四氫生物蝶呤(BH4),作為一種有效的抗氧化劑,抑制脂質過氧化。
二氫乳清酸脫氫酶(DHODH) 在線粒體中通過類似FSP1的機制抑制鐵死亡。
下表總結了鐵死亡的主要調控因子及其功能:
表:鐵死亡關鍵調控因子及其功能
調控因子 | 功能 | 調控方向 |
GPX4 | 還原脂質過氧化物 | 負向調控 |
系統Xc- (SLC7A11) | 胱氨酸攝取,GSH合成 | 負向調控 |
FSP1 | 泛醇再生,中和脂質自由基 | 負向調控 |
GCH1 | 產生BH4,抗氧化 | 負向調控 |
ACSL4 | PUFA-PLs合成 | 正向調控 |
NOXs | ROS產生 | 正向調控 |
NANS | 抑制NF-κB-FTH1通路 | 正向調控 |
3、新興調控節點:NANS與NOXs
最新研究發現,N-乙酰神經氨酸合成酶(NANS)通過調控鐵穩態在結直腸癌鐵死亡中發揮重要作用。NANS通過直接結合TAK1的N端結構域,阻斷TAK1-TAB1復合物形成,抑制TAK1的K63泛素化和磷酸化,進而抑制下游NF-κB信號通路。NF-κB信號通路的下調減少了其對鐵蛋白重鏈1(FTH1)的轉錄激活,FTH1作為鐵儲存蛋白,其表達降低導致細胞內游離鐵增加,促進鐵死亡發生。NADPH氧化酶(NOXs)家族成員(NOX1、NOX2和NOX4)也被證實通過不同機制促進鐵死亡。NOX1在p53蛋白調控下與二肽基肽酶4(DPP4)結合介導質膜脂質過氧化;NOX4受EGFR-MAPK信號通路誘導表達,產生H?O?參與芬頓反應。
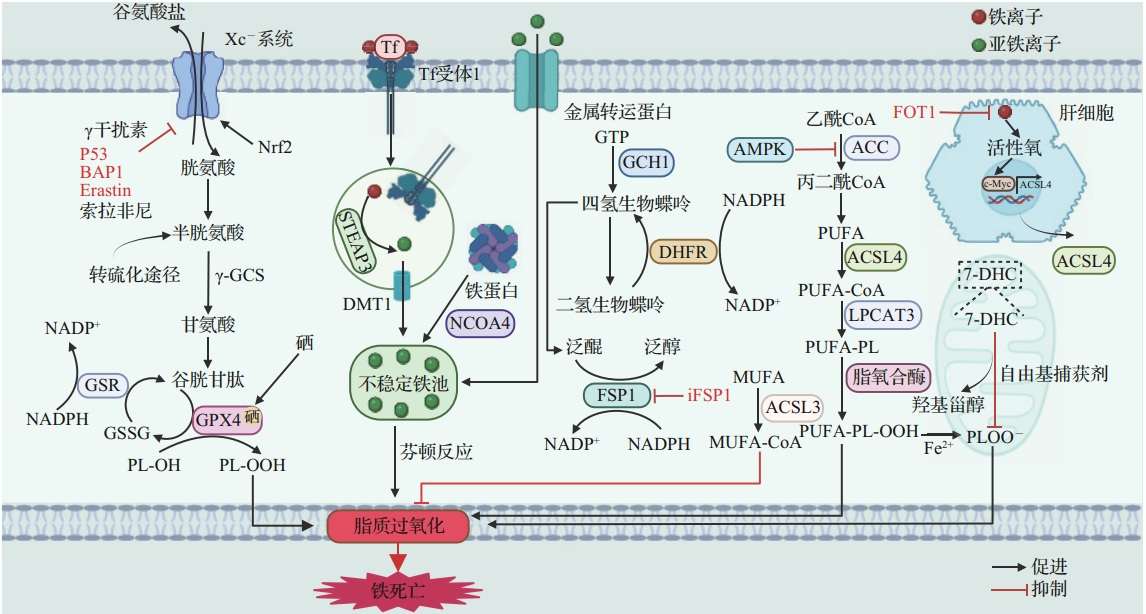
圖2 鐵死亡信號通路在肝病中的調控機制示意圖[2]
三、鐵死亡研究策略與技術
1、基因篩選與分子鑒定
CRISPR-Cas9全基因組篩選是發現鐵死亡新型調控因子的有力工具。例如,研究人員通過代謝酶文庫篩選,發現了NANS是鐵死亡的正調控因子。RNA干擾技術可用于靶向驗證特定基因功能。一項研究通過合成靶向HDACs家族(HDAC1-11)的siRNA文庫篩選,發現沉默HDAC1可顯著促進Erastin誘導的鐵死亡。分子生物學技術如染色質免疫共沉淀(ChIP)可用于研究轉錄因子與靶基因啟動子的結合情況。研究表明,NF-κB亞基RelA可直接結合FTH1啟動子,而NANS缺失增強這種結合。
2、細胞死亡確認與表型分析
鐵死亡特異性抑制劑是確認鐵死亡的關鍵工具。Ferrostatin-1和Liproxstatin-1是常用的鐵死亡抑制劑,若它們能逆轉細胞死亡,則表明死亡方式可能是鐵死亡。
脂質過氧化檢測是鐵死亡表征的核心指標。C11-BODIPY??1/??1探針可用于檢測細胞內脂質過氧化水平。
細胞內鐵離子檢測可使用Phen Green SK、RPA、RhoNox-1等熒光探針。
電鏡觀察可揭示鐵死亡獨特的超微結構特征:線粒體收縮、膜密度增加、嵴減少或消失。
3、先進成像技術
最新研究表明,熒光壽命成像顯微鏡(FLIM) 結合極性敏感熒光探針(如SBD-CH)可實時監測鐵死亡過程中內質網極性變化,為早期檢測提供新方法。這種技術優勢在于熒光壽命是熒光分子的固有特性,與探針濃度無關,能避免傳統強度型探針的成像失真問題。
四、疾病關聯與靶向治療前景
1、癌癥治療中的雙面劍
鐵死亡在癌癥中扮演雙重角色:一方面,誘導鐵死亡可抑制腫瘤生長;另一方面,某些腫瘤細胞可通過上調抗氧化通路獲得鐵死亡抵抗。在結直腸癌中,NANS表達水平與患者預后顯著相關。研究發現,在鐵死亡壓力下,CDK1介導的NANS S275位點磷酸化,觸發UBE2N依賴的泛素化降解,導致NF-κB-FTH1軸激活和鐵死亡抵抗。聯合使用CDK1抑制劑(如RO-3306)與鐵死亡誘導劑,在動物模型中顯示出協同抗轉移效果。
2、非酒精性脂肪性肝病(NAFLD/NASH)
鐵死亡在NAFLD/NASH發生發展中起關鍵作用。生物信息學分析鑒定出ZFP36、ATF3、SOCS1、IL-6、PTGS2、JUN等9個NASH鐵死亡關鍵基因。實驗證實,游離脂肪酸(FFA)處理的HepG2細胞中,c-jun、ZFP36、ATF3、IL-6蛋白表達升高,脂質過氧化增強。抑制鐵死亡幾乎可抑制NASH發生。
3、神經退行性疾病
在帕金森病、阿爾茨海默病等神經退行性疾病中,鐵蓄積和脂質過氧化參與神經元死亡過程。GPX4失活導致脂質過氧化物(如4-HNE)累積,觸發神經元膜結構破壞。轉錄因子AP-2γ與SP1的協同激活可上調GPX4表達,這一通路為神經保護提供了新靶點。
五、挑戰與未來方向
當前鐵死亡研究面臨多項挑戰:鐵死亡與其他細胞死亡方式的crosstalk復雜;組織特異性調控機制尚不明確;靶向藥物的遞送效率和特異性不足。未來研究重點應包括:開發時空特異性誘導劑;探索組織特異性調控網絡;優化納米遞送系統提高靶向性;深入研究翻譯后修飾(如磷酸化、泛素化、乙酰化)調控機制。隨著對鐵死亡機制理解的深入,以及研究技術的不斷創新,靶向鐵死亡的治療策略有望在癌癥、神經退行性疾病和代謝性疾病等領域取得突破性進展。
參考文獻
[1] Signaling pathways and defense mechanisms of ferroptosis. DOI: 10.1111/febs.16059
[2] Ferroptosis and liver diseases. DOI:10.3724/zdxbyxb-2024-0566
鐵死亡研究產品推薦:
貨號 | 名稱 | 規格 |
abs580233 | 活性氧ROS檢測試劑盒(紅色熒光) | 500T |
abs90072 | 普魯士藍染色試劑盒(三價鐵,增強型) | 20mL×4 |
abs126100 | Rabbit anti-4 Hydroxynonenal Polyclonal Antibody | 100uL |
abs154673 | Mouse anti-GSTO1 Monoclonal Antibody(JMMR-2558) | 100uL |
abs810466 | Cisplatin | 50mg |
abs810744 | Erastin | 5mg |
abs47006920 | Glutathione | 20mg |
abs810754 | Liproxstatin-1 | 5mg |
abs42007826 | 菲啰嗪一鈉鹽(鐵離子檢測指示劑) | 1g |
【免責聲明】本篇文章來源于網絡公開信息,由AI生成,若不慎侵權,請及時聯系,我們將第一時間配合處理,不承擔任何法律責任。
好消息!Absin文獻獎勵重磅升級!
Absin產品線:
爆款產品:試劑盒(mIHC、IHC、凋亡、ELISA、ChIP、Co-IP、TR-FRET、生化檢測、殘留檢測、多因子檢測);細胞培養(類器官試劑盒+基質膠,胎牛血清+培養添加劑+細胞因子)、分化試劑盒;分子(mRNA合成服務+提取試劑盒);化合物大包裝;輔助試劑、耗材/儀器、定制服務(抗體/多肽/蛋白/標記/檢測)...
特色產品:雞胚提取物CEE、B27、N2、霍亂毒素B亞單位CTB、牛腦垂體提取物BPE、百日咳毒素PTX、重組人胰島素Insulin、人源低密度脂蛋白LDL...